Nat. Comput. Sci. | 面向治疗性抗体设计的双阶段生成优化框架
Nat. Comput. Sci. | 面向治疗性抗体设计的双阶段生成优化框架

DrugAI
发布于 2026-04-20 13:16:00
发布于 2026-04-20 13:16:00
DRUGONE
实现治疗性抗体的临床应用,需要在多个关键属性之间取得平衡,包括抗原结合特异性、黏度、清除率以及免疫原性等。然而,现有方法往往依赖多步筛选或单一目标优化,难以同时兼顾这些复杂性质。
研究人员提出了DualGPT-AB,一种双阶段生成优化框架,用于在多属性约束下设计抗体序列。该方法通过条件生成模型学习序列与性质之间的关系,并结合强化学习策略在序列空间中进行高效探索。实验结果表明,该方法能够生成满足多重约束的抗体CDRH3序列,并在HER2靶点任务中表现出优异性能。实验验证进一步显示,部分设计抗体在肿瘤杀伤能力上优于临床抗体Herceptin,证明了该框架在抗体设计中的潜力。

单克隆抗体已成为治疗癌症和自身免疫疾病的重要药物,其功能依赖于对特定抗原表位的高效识别与结合。在抗体结构中,重链互补决定区3(CDRH3)由于高度多样性,对抗原结合特异性具有决定性作用。
然而,仅具备良好的结合能力并不足以保证抗体的临床可用性。抗体还需要具备良好的开发性属性,例如低黏度、适当的电荷分布、良好的稳定性以及低免疫原性。这些属性之间往往存在冲突,使得抗体设计成为一个复杂的多目标优化问题。
尽管已有方法尝试利用进化算法、强化学习或生成模型进行抗体设计,但这些方法通常将不同属性视为独立目标,缺乏对序列与属性之间复杂关系的建模能力。因此,研究人员提出一种新的思路:通过生成模型直接学习“序列—多属性”之间的耦合关系,从而实现高效设计。
方法
研究人员构建了DualGPT-AB框架,其核心是一个双阶段条件生成模型。在第一阶段,利用大规模抗体数据库构建带有限属性标注的数据集,训练一个初始生成模型,使其能够生成满足基础属性的序列。在第二阶段,引入强化学习,通过奖励函数引导模型在更复杂的多属性空间中探索,并逐步构建包含扩展属性的数据集。
最终,通过增强生成模型学习完整的“序列—多属性”关系,实现能够同时满足多种设计目标的抗体序列生成。
结果
DualGPT-AB整体框架
DualGPT-AB通过双阶段策略实现从基础生成到多属性优化的过渡。第一阶段通过已有数据学习基本序列分布,第二阶段通过强化学习不断优化生成策略,使模型逐步逼近目标属性空间。
这一框架的关键在于,将属性信息嵌入到生成过程中,使模型能够在生成序列时直接考虑多种约束,而非后处理筛选。
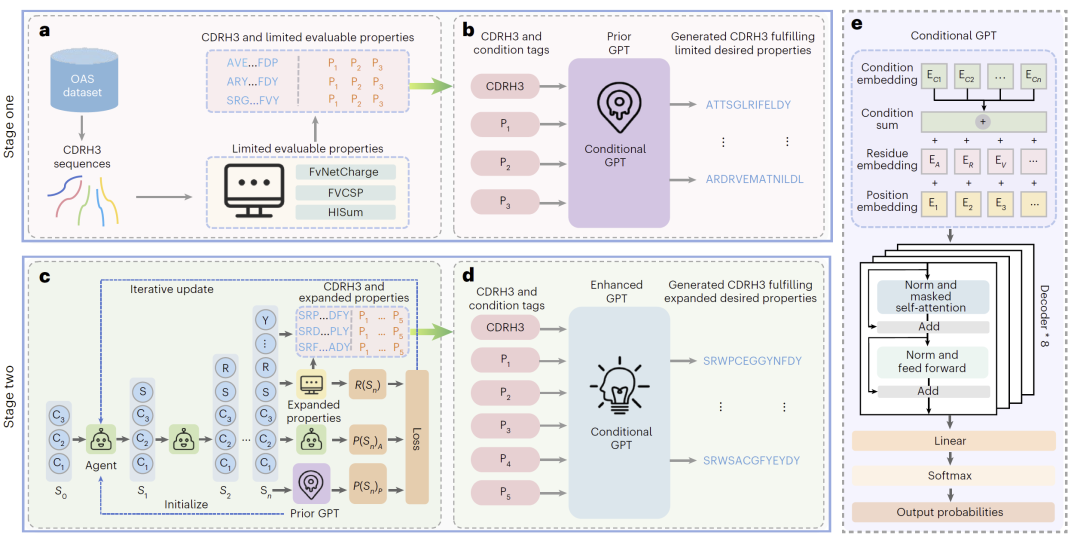
图1:DualGPT-AB整体框架与双阶段训练流程。
多属性约束下的性能优势
在多属性约束条件下,DualGPT-AB显著优于现有方法。在生成的抗体序列中,同时满足所有五项关键属性的比例达到78.2%,远高于其他方法。
进一步分析表明,该方法在不同属性组合下均保持稳定表现,说明其在多目标优化中具有较强鲁棒性。这一能力对于抗体设计尤为重要,因为实际应用中往往需要同时满足多个严格条件。
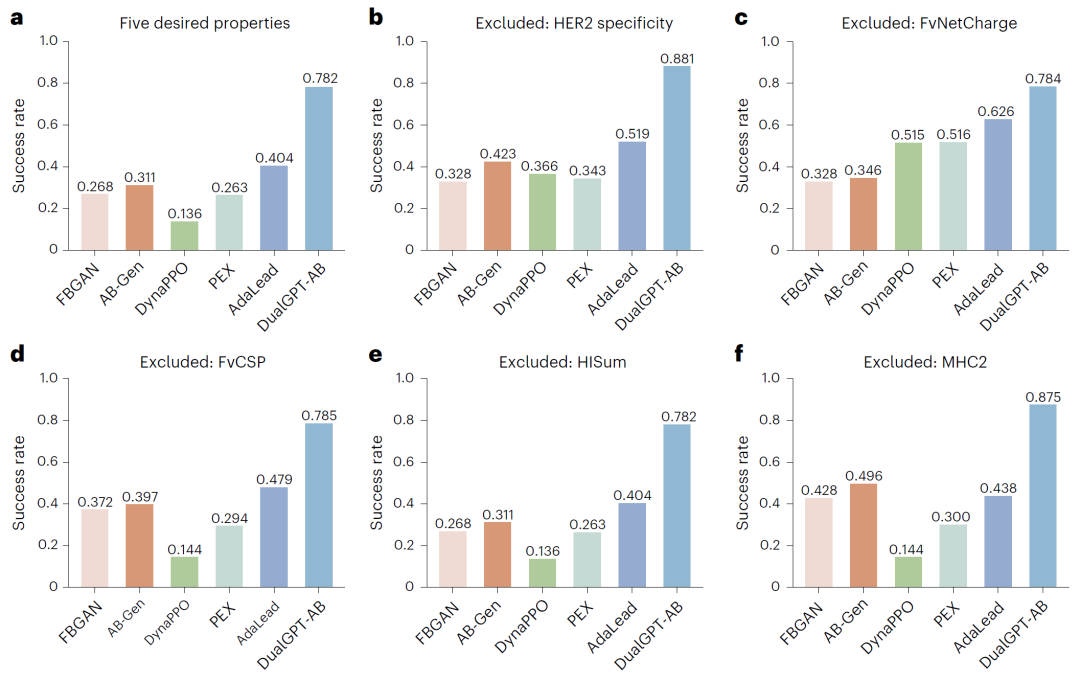
图2:多方法比较与成功率分析。
双阶段策略的有效性
通过对不同阶段生成结果的分析可以发现,第一阶段模型能够有效学习基础属性分布,但在复杂属性(如HER2特异性)方面表现有限。而第二阶段模型在强化学习引导下,显著提升了对多属性的综合优化能力。
最终模型在所有目标属性上均表现出更集中且符合要求的分布,并将成功率从几乎为零提升至接近80%。
这一结果证明,双阶段设计在复杂生物序列优化中具有关键作用。
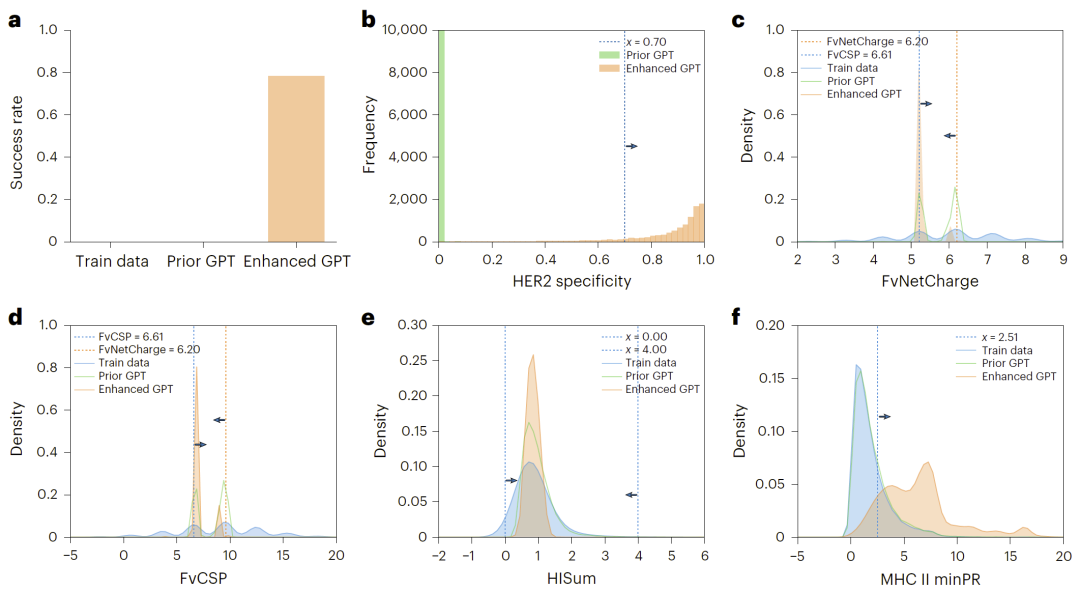
图3:不同阶段属性分布与成功率变化。
抗体序列库的结构与性质分析
研究人员利用DualGPT-AB生成大规模抗体序列库,并通过溶解性筛选获得高质量候选集合。分析显示,该序列库在关键残基位置具有明显保守性,同时整体结构具有较高多样性。
结构预测进一步表明,不同序列在三维结构上表现出显著差异,说明模型不仅能够生成符合约束的序列,还能够探索多样化结构空间。
此外,序列组成分析揭示某些氨基酸(如Gly和Tyr)在功能位点中富集,提示模型已学习到与抗原结合相关的关键模式。
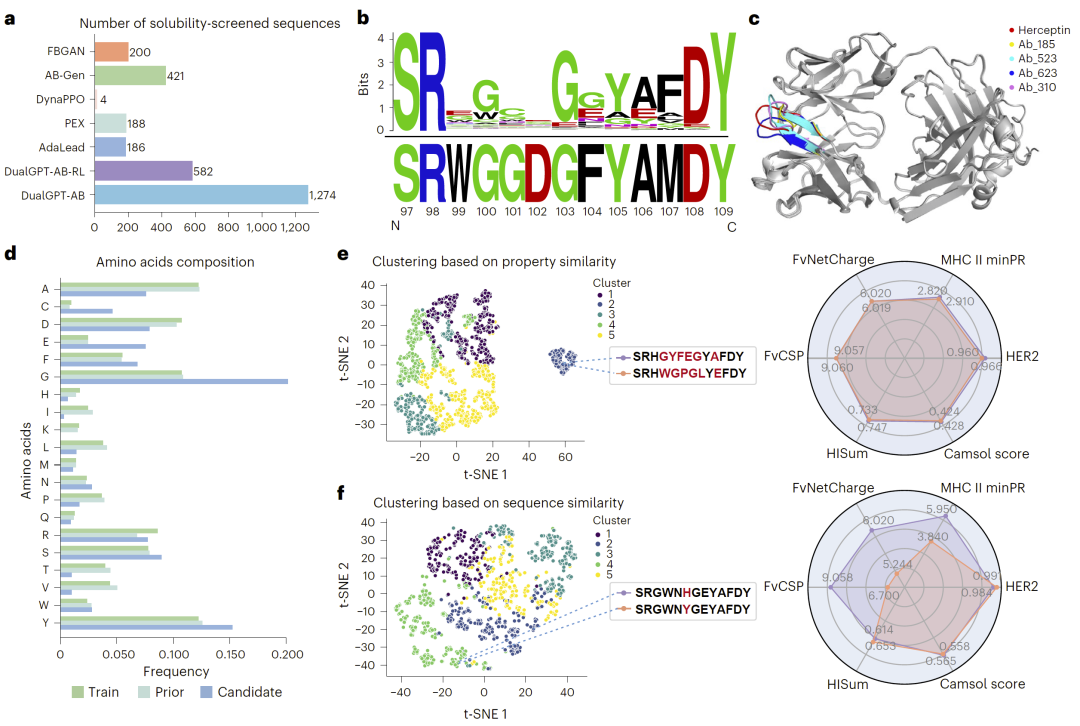
图4:序列库特征、结构多样性与聚类分析。
计算验证:高亲和力抗体设计
通过结构预测与结合能计算,研究人员评估了生成抗体的结合能力。在随机选取的100个候选中,超过一半表现出与Herceptin相当的结合能力,部分甚至更强。
进一步分析发现,序列差异并不一定降低结合能力,说明模型能够在保持功能的同时探索新的序列空间。这对于发现新型抗体具有重要意义。
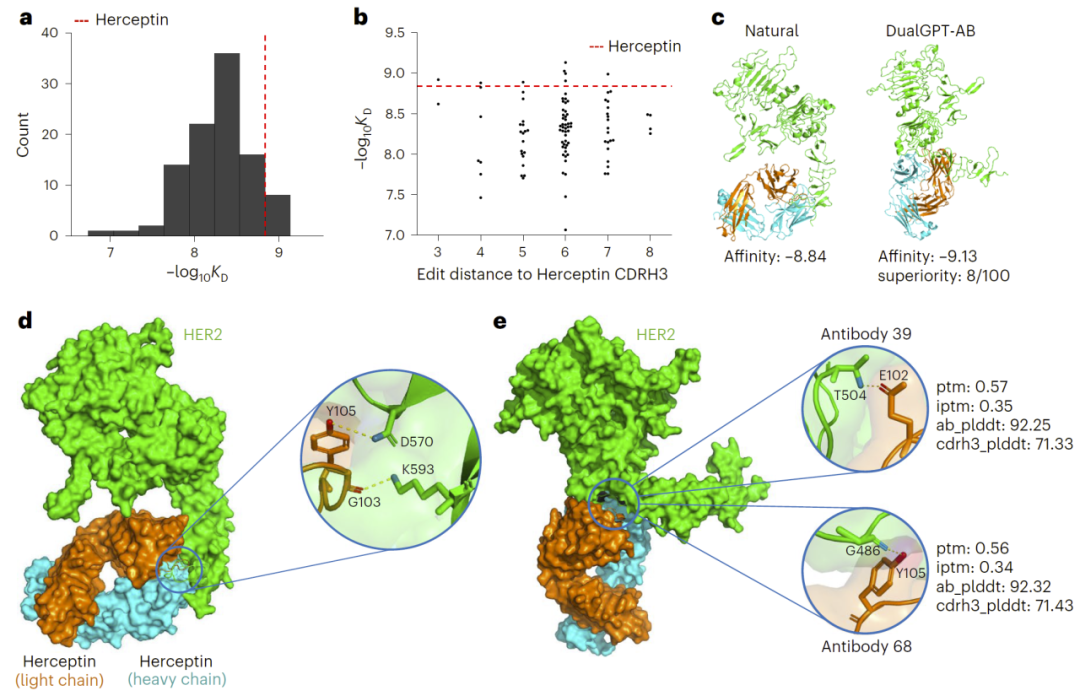
图5:结合亲和力预测与结构相互作用分析。
实验验证:抗体功能提升
在体外实验中,研究人员验证了部分候选抗体的功能。结果显示,设计抗体不仅具有良好的HER2结合能力,还在细胞毒性实验中表现出优于Herceptin的肿瘤杀伤能力。
特别是在ADCC和CDC实验中,一些候选抗体表现出更强的免疫效应,表明该方法不仅优化结合能力,还可能提升整体功能。
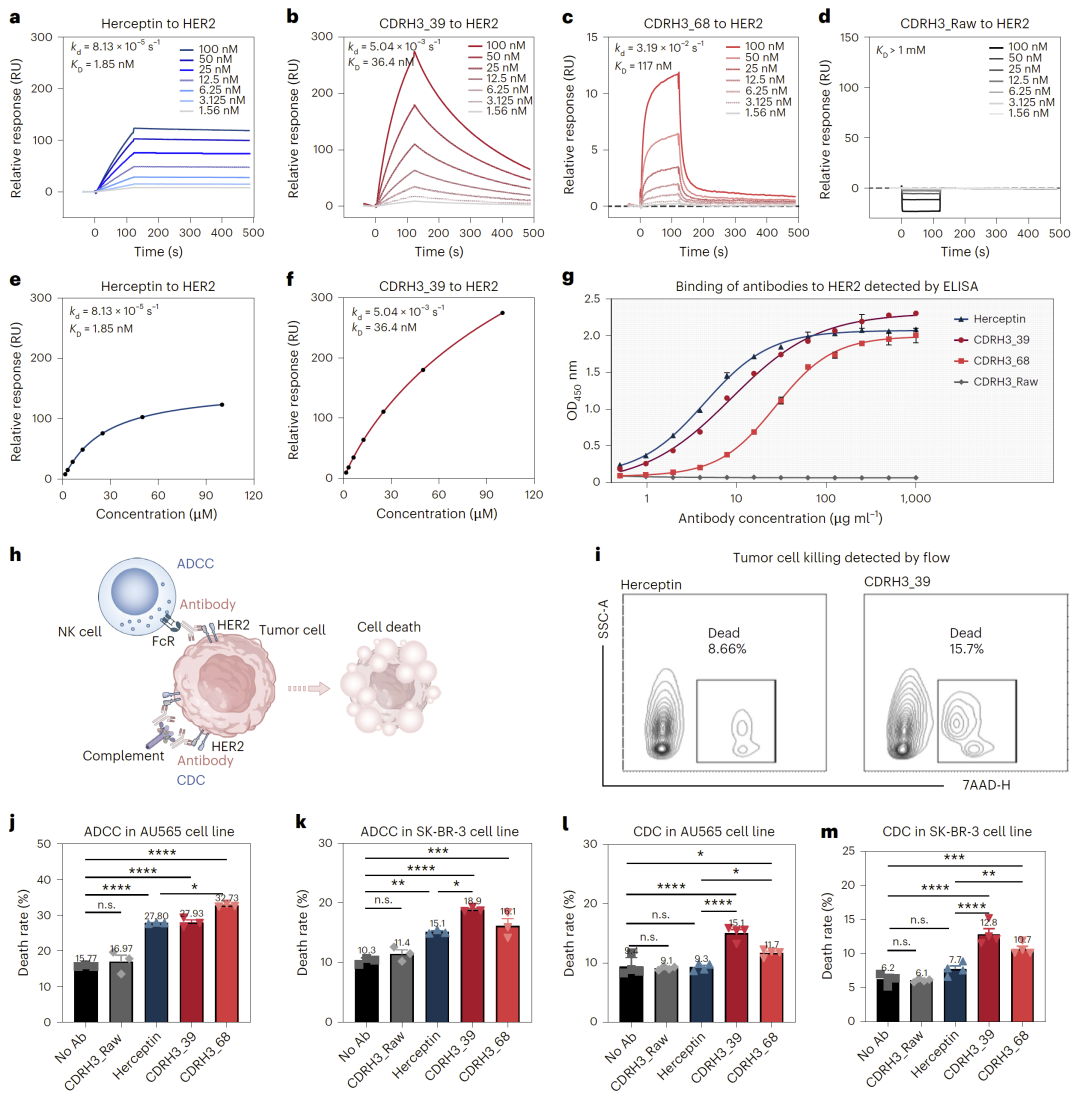
图6:SPR、ELISA与细胞杀伤实验验证。
讨论
本研究提出的DualGPT-AB框架,将抗体设计问题转化为一个多属性条件生成问题,通过双阶段策略有效解决了数据稀缺与多目标优化的挑战。
相比传统方法,该方法能够直接学习序列与多属性之间的复杂关系,从而避免简单加权或逐步筛选带来的信息损失。这种端到端的建模方式显著提升了设计效率与成功率。
值得注意的是,抗体功能不仅由抗原结合决定,还受到变构效应等因素影响。例如,本研究中部分抗体在结合能力不占优势的情况下,仍表现出更强的肿瘤杀伤能力,这提示抗体设计需要综合考虑结构与功能的耦合机制。
尽管该方法仍依赖于特定靶点的预测模型,但其模块化设计使其能够扩展至其他抗原系统。未来结合物理建模与跨任务学习,有望进一步提升模型泛化能力。
总体而言,DualGPT-AB为AI驱动的抗体设计提供了一种高效且可扩展的新范式,在药物发现领域具有重要应用前景。
整理 | DrugOne团队
参考资料
Xie, D., Chen, S., Zeng, X. et al. DualGPT-AB: a dual-stage generative optimization framework for therapeutic antibody design. Nat Comput Sci (2026).
https://doi.org/10.1038/s43588-026-00976-0
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-18,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

