Nat. Biotechnol.|人工智能-药物混合体的创新与政策挑战
Nat. Biotechnol.|人工智能-药物混合体的创新与政策挑战

DrugAI
发布于 2026-04-20 13:14:27
发布于 2026-04-20 13:14:27
2026年3月17日,克里特大学、哈佛大学、哥本哈根大学等机构的研究人员在《Nature Biotechnology》上发表文章,题为“Innovation and policy challenges of AI–drug hybrids”。
背景
医疗技术的一个新前沿正悄然临近。在这个前沿中,人工智能应用与药物紧密相连,以至于没有AI,这些药物实际上将无法使用。AI应用程序可以挖掘数据源,评估患者更广泛的临床背景,并通过预测特定药物的最佳摄入方式来辅助患者和医生。专利文件已清晰揭示了这一趋势。例如,辉瑞的专利申请WO2023119208A1描述了一种“药物+应用”技术:应用通过部署机器学习模型,基于健康数据判断患者服用特定药物后是否可能出现不良健康状况,并触发通知,提醒患者及其临床医生重新安排注射时间或调整剂量,从而提高药物的疗效和/或安全性。
这一趋势并非完全前所未有。此前已有将药物与复杂的伴随诊断和医疗设备相结合的产品,例如“仿生胰腺”,它可以监测患者血糖并在适当时机自动给药。但新型组合将这一理念大幅推进——从自动化转向复杂的个性化定制。早期应用包括高效但有毒的肿瘤药物,患者仅会在应用提示特定时刻副作用可耐受时才服用。监管机构已开始关注这一趋势。毫无疑问,这些发展对大多数疾病(不仅是肿瘤)都蕴藏着巨大潜力,使药物能够更有效地使用并用于更多用途。然而,它们也给创新政策和患者可及性带来了新的挑战。掌握临床试验数据的企业,或许能够获得长期的市场主导地位。
AI-药物混合体的兴起
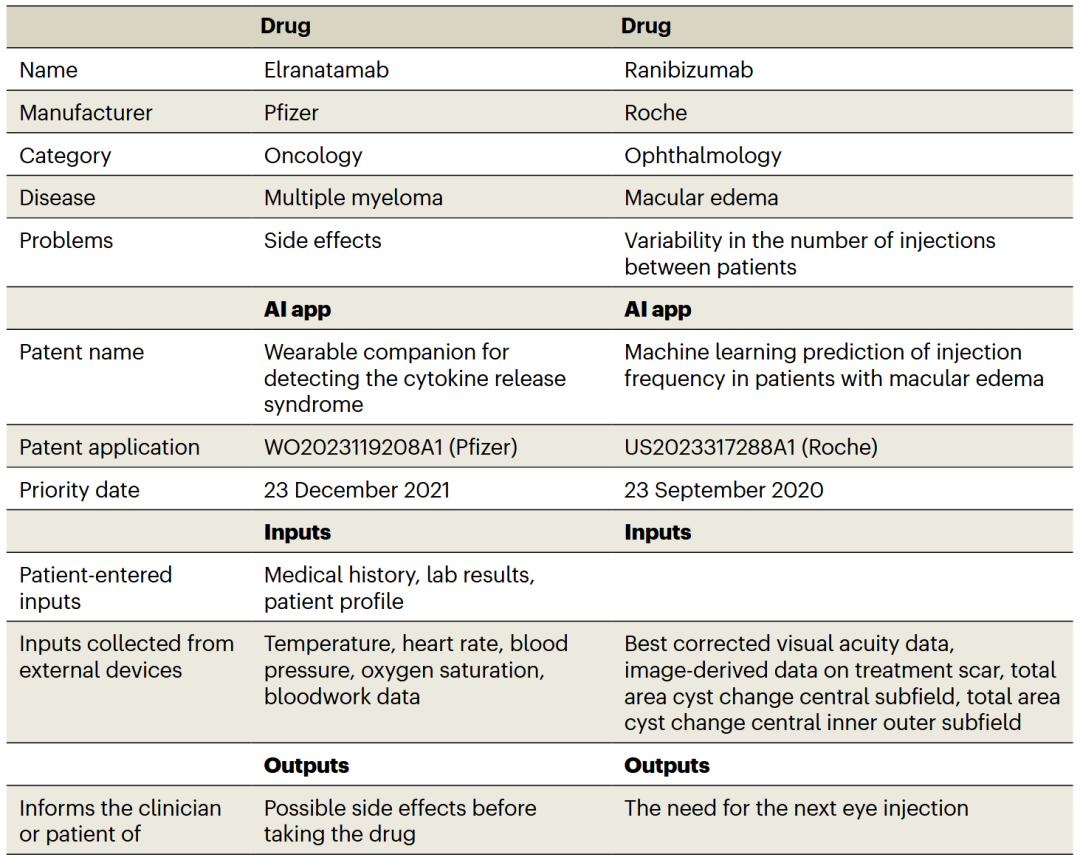
研究AI与药物之间的耦合并非易事。尽管有大量文献探讨AI如何与药物递送系统协同工作,企业也公开表示对AI的兴趣,但市场上尚无内置AI的药物。然而,专利申请却展现了不同的图景。专利是创新的重要早期指标,有助于开展前瞻性扫描,发现重大发展的早期迹象,从而帮助政策制定者管理风险、把握机遇。专利申请表明,未来AI将与特定药物协同工作,仿佛它们是一个整体产品。研究者将此类产品称为“AI-药物混合体”。在这些混合体中,AI应用以无监督的方式持续与药物协调运行,独立提供定制化的预测,以增强药物的安全性和/或有效性。例如,考虑分别由辉瑞和罗氏提交的专利申请WO2023119208和US2023317288A1,其技术、配套药物及范围概见表1。
表1 AI应用的描述
案例一:辉瑞的多发性骨髓瘤药物
辉瑞的专利申请WO2023119208针对其双特异性抗体药物埃兰他单抗(elranatamab)。该药用于治疗多发性骨髓瘤,但因副作用较大,目前仅被批准作为最后治疗手段。根据专利申请摘要,该技术描述了一种“数字药物”,患者可下载并开始使用,包括可穿戴设备及其应用、移动设备应用等。利用从这些设备被动收集的数据,AI使患者或临床医生能够了解每次使用埃兰他单抗时是否会出现副作用。这有助于临床医生判断特定副作用是在好转还是恶化,从而调整患者服用的药物剂量,决定让患者出院进行居家监测,还是留在医院观察。具体操作模式为:治疗前,应用获取来自各种追踪设备(手机、健身追踪器、智能手表、血液监测设备)的输入数据,评估副作用的严重程度,并通知医生,使其能够决定是调整剂量、让患者出院,还是将患者留在医院观察。图1概述了埃兰他单抗的操作模式。
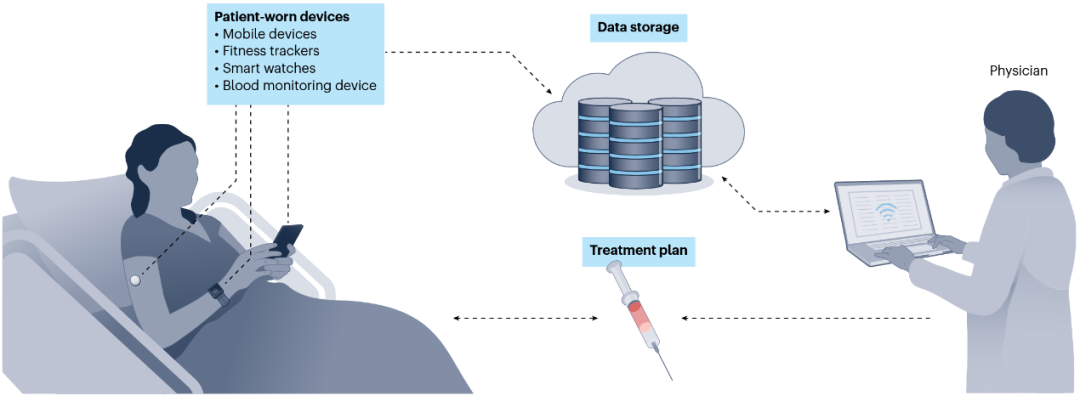
图1 辉瑞专利申请WO2023119208A1中“药物+应用”技术的操作模式
案例二:罗氏的黄斑水肿药物
罗氏的专利申请US20230317288A1针对黄斑水肿。这种疾病需要长期治疗,患者需前往医院接受罗氏药物雷珠单抗(ranibizumab)的眼部注射。由于患者之间的异质性可能导致注射次数不同,患者的长期治疗管理颇具挑战性。该专利描述了一款应用,它利用来自眼科检查(由罗氏的另一款AI智能手机应用执行)的数据,来预测患者使用雷珠单抗的治疗频率。
竞争优势
尽管AI-药物混合体看起来完全是积极的发展,但数字化可能赋予这些产品显著的竞争优势。要创建此类混合体,需要两种投入。第一种是算法,必须针对具体问题重新构建——这成本低廉且易于实现。第二种是训练数据。例如,US20230317288A1明确指出:“机器学习模型是使用由雷珠单抗的BRAVO(NCT00486018)和CRUISE(NCT00485836)三期临床试验数据形成的训练数据进行训练和测试的。”使用临床试验数据并不令人意外。由于专利详细描述了在受控环境下发生的药物-患者相互作用,临床试验数据提供了最接近真实情况的表现形式。BRAVO和CRUISE试验涉及789名“继发于视网膜静脉阻塞的黄斑水肿”患者,按照详细标准精心挑选,在六个月内接受不同剂量的治疗,并再接受六个月的观察。
如果没有进行这些大规模试验,要重建类似的训练数据集将非常昂贵,而且商业竞争对手没有理由去承担这样的任务。这限制了缺乏此类数据的竞争对手对该应用进行计算复现的能力,从而使掌握临床试验数据的企业获得了竞争优势。此外,企业还可以通过合同或技术手段,将该应用的下载限制于服用原研药的患者(而非服用仿制药的患者),从而进一步限制那些试图搭便车使用该应用、但缺乏内置AI组件的药物的竞争。
披露缺口
鉴于临床试验数据在训练AI-药物混合体方面的优势,研究者担心,数字化不仅会影响当前竞争,甚至可能在这些应用的相关专利到期后仍然限制竞争,从而阻碍仿制型AI-药物混合体的市场进入。原因在于训练数据的不完全披露。所讨论的专利申请仅提及了训练数据集,但并未公开该数据集。例如,US20230317288A1描述其训练数据集基于雷珠单抗的临床试验,但没有提供进一步详细说明。WO2023119208也仅将训练数据概述为“生物数据……实验室分析数据……人口统计学信息、病史……可能影响双特异性抗体治疗的其他医疗保健属性”。这种披露不足限制了竞争对手对仿制版本应用进行适当训练的能力。
这种披露缺口并非个例。在一组相关的已授权医疗AI技术专利中,只有不到70%公开了此类AI训练的具体细节。虽然欧洲专利局近期强调,必须至少以足够的细节披露一个工作示例,并要求提供有关训练数据的足够信息,但同时也认为,不需要完全公开所有训练数据本身。
持续演进
更为关键的是,AI-药物混合体并非静态的。从专利提交之时起,其软件组件就可能发生变化,相应地提高其疗效。以雷珠单抗为例:一旦患者开始使用混合型雷珠单抗,其应用将不断向罗氏提供辅助数据。与临床试验数据不同,这些补充数据涵盖了受控环境之外的药物-患者相互作用。由于该数据集融入了真实世界证据,它可以用于不断完善应用的预测,以应对真实世界的情景。
如果专利中描述的应用在训练时使用了临床试验数据,那么这种辅助数据集可用于对其进行优化和改进,从而进一步使其免受竞争。因此,即使完全公开了临床试验数据,混合型雷珠单抗也将优于任何后来获得市场批准的、仅使用已提交数据(而非专利有效期内收集的辅助数据)进行训练的仿制药——后者属于商业秘密。
这意味着,即使专利到期、竞争对手可以自由复制AI-药物混合体,他们仍然缺乏通过用户交互积累的数据。因此,即使竞争对手确实创建了自己的仿制应用,它们与AI-药物混合体的当前应用相比仍然是劣质的。更不用说,对于需要关联AI应用的适应症,监管机构可能甚至不会批准此类仿制药;即使获批,它们对患者或医生而言也可能不构成可接受的替代品。
现有法规的不足与可能的出路
理论上,更多披露的要求也可能来自其他渠道,例如欧洲药品管理局通过《欧洲临床试验法规》的透明度要求。该法规要求公开共享临床试验数据,这可以为竞争对手提供应用基础训练所需的数据。然而,共享的数据代表的是提交给监管机构时的药物版本,而不是混合体当前版本的数据。其他新法规——如《医疗器械法规》、《欧洲人工智能法案》或即将出台的《欧洲健康数据空间》——可能通过要求技术文档和透明度来促进训练数据的进一步披露。然而,除非对这些法规进行修订以解决训练数据持续更新的问题,否则该问题将持续存在。
合成数据或许可以通过人工重建所需数据来部分解决这一问题。但生成合成数据需要对其所要重建的对象有深入了解。虽然可以利用公开的临床试验描述来重建临床试验数据,但企业在优化和改进应用过程中所使用的用户数据将无法公开获取,因此为应用重建一个足够好的替代品似乎仍然不可行。
最后,部分数据仍将受到商业秘密、监管数据独占权、市场独占权以及个人数据保护法律(如《通用数据保护条例》)的保护。企业只会披露为合规所绝对必要的数据,并采用分层数据保护和商业秘密策略。欧盟内部正在讨论是否将强制许可的适用范围扩大到包括获取受保护的监管数据和商业秘密。但这些提议面临行业的强烈反对。此外,强制许可通常仅在定价过高的情况下作为谈判工具,并作为特殊情况(如反垄断违法、突发危机或公共卫生需求)下的最后手段。
总结
将药物与人工智能相结合,使得拥有临床试验数据的企业能够创建并持续升级AI-药物混合体。与此同时,这些药物的非静态特性及其与持续收集的数据之间的紧密联系,将为它们带来持久的竞争优势。这降低了风险,提高了回报。研究者呼吁,政策制定者需要关注AI-药物混合体所带来的新型竞争动态,在鼓励创新的同时,确保患者能够以可负担的价格获得这些前沿疗法。否则,数字化可能无意中从“赋能患者”变成“锁定市场”,让少数巨头凭借数据壁垒长期主导特定药物的治疗生态。
参考链接:
https://doi.org/10.1038/s41587-026-03041-3
--------- End ---------
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-16,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

